患者が理解して受ける脳の放射線治療
『脳機能を保てる放射線治療 海馬回避(1)』
医療法人北斗 北斗病院副院長・放射線治療科部長 岸 和史
原発の脳腫瘍はそんなに多く見られず、多くが転移性のものと伺っている。そういう理由からか、10年以上になる当会の活動でも、脳腫瘍の相談はそんなに多くない。最近、3例ほどの脳腫瘍の相談を受け、幸いいい結果を得ており、「がんは放射線でここまで治る 第2集」にも脳腫瘍の事例を収載させていただいた。
今回は北斗病院副院長・放射線治療科部長の岸 和史先生に、「脳機能を保てる放射線治療」についてご寄稿いただいた。
長文なので2週にわたって連載させていただきます。
今回は北斗病院副院長・放射線治療科部長の岸 和史先生に、「脳機能を保てる放射線治療」についてご寄稿いただいた。
長文なので2週にわたって連載させていただきます。
(會田 昭一郎)
本論
「脳転移への放射線治療の選択」
いま、目の前にある治療の選択肢は、理想的な治療なのでしょうか?
あるいは現実的な選択肢の中で、本人にとってベストなのでしょうか?
このシリーズでは脳転移への放射線治療の選択をガイドします。
これまでの放射線治療は腫瘍細胞にダメージを与える事を優先してきました。そのための正常組織の犠牲もやむを得ないとして受け入れられてきました。本来、脳への照射の理想は、脳機能を守り、腫瘍を制御することでなければならない筈です。
脳への照射方法の話
この章は、脳転移への放射線治療を、選択していただけるようにお話します。第一部は、脳転移の予防のための放射線治療を、第二部は脳転位がすでにある脳転移巣の治療をお話しします。
第Ⅰ部.予防のための照射。
予防的照射
当初からあきらかな病巣がなかった領域に対して放射線治療を行うことを予防的照射と呼びます。なお、一度病巣があって何かの治療後に今は肉眼的に見えなくなった部分への照射は、予防とは呼ばずに、後治療としての照射、"アジュバント"照射と呼んで区別しています。手術で、病巣を除去した後への術後照射もアジュバント照射の一つです。予防的照射は普通は全脳に行います。
1.予防的全脳照射
脳はまだ画像的にも病巣がないが、転移が発生してくる確率が高い場合があります。それらには、限局期小細胞肺癌で肺病変が完全に制御された(完全寛解)獲得後や、急性白血病の完全寛解後などがあります。これらでは疫学的なエビデンスも十分揃い、標準治療に採用されています。
種まき元になる原発病巣が完全寛解の状態で、それでも統計的に30%以上の確率で脳転移が発生すると予測される時、その脳転移の発生頻度を予防照射で10%以下に低下させられるデータが十分あるので、標準治療になったのです。
予防的全脳照射の一回線量と照射回数
総線量では、2Gyx15回=30Gyや3Gyx10回=30Gyがよく用いられます。脳機能障害等や脱毛の副作用があります。
脱毛は頭皮毛根への線量の多寡で決まります。
普通の予防的全脳照射で、海馬(近時記憶などの中枢)への照射を回避をしない場合は、30%の方に健忘などの脳機能障害が発生すると報告されています。小児の場合には就学・学習能力への影響が深刻な問題として議論されています。
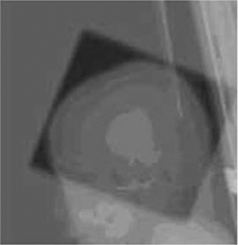
図1A 予防的全脳照射法
この図は従来の方法を示しています。海馬は回避されません。後述のトモセラピーに比べると均質な線量分布の均質性は高くありません。
海馬について(図2)
脳の中は寄せ木細工のように色々な部分に分解できます。
海馬はタツノオトシゴのような形をしています。海馬という呼び名はタツノオトシゴを"海のお化け馬"(ÌΠΠÓΚαμΠΟς , ÏΠΠΟς = 馬 + ΚáμΠΟς = 海の怪物)というギリシア語に由来します(鼻が馬面です)。
海馬は歯状回とアンモン角からなり、大脳辺縁系に属します。辺縁系の一部とはいうものの中核的な働きをしています。新しい情報の抽出、協調、固定は海馬で行われ、新しい記憶として形成されます。海馬と大脳皮質の役割を喩えると、海馬は仕分け・関連・意義付け、そして大脳皮質が倉庫です。
海馬がうまく機能しなくなると、学習障害、近時記憶障害(昔のことは"倉庫"にあるので思い出せる)、方向や位置認識能力障害をきたします。認知症の方が場所がわからなくなるのは、この障害です。
これらの脳機能障害を起こす要因は、放射線や薬剤だけでなく、もっと一般的に、ストレス、鬱病、アルツハイマー病などたくさんあります。MRI等で、障害を起こした海馬が小さく萎縮している様子が観察されることがあります。細胞が減ってしまうと小さくなってしまうのですね。
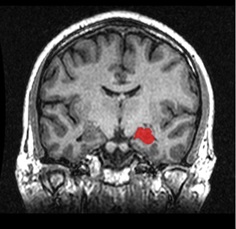
図2 MRI画像。海馬。
海馬は脳細胞の密度の高い「灰白質」の塊なので、MRI画像で海馬部分は濃い灰色だ(右。左側の海馬は赤くペイント)。白く見えるのは「白質」で神経繊維の多い部分。
http://en.wikipedia.org/wiki/File:MRI_Location_Hippocampus_up..png
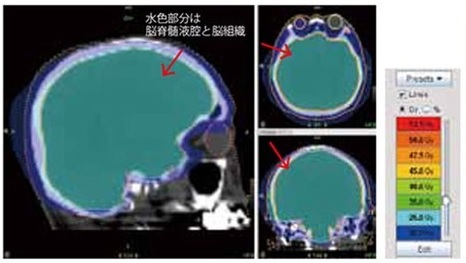
図1B トモセラピーでの全脳照射
この図でも海馬は回避していません。線量分布は均質で、脳脊髄液腔と脳組織が水色の領域になっています。骨と皮膚はブルー(25-15Gy)か色無し(15Gy以下)。ブルー以下であれば通常、毛髪は保たれます。
2.海馬回避全脳照射 (Hippocampus sparing PCI : HS-PCI)
脳転移は均等に分布するわけではありません。実は海馬に転移する確率は低いのです。従って海馬を外せるなら外して予防照射してはどうか、と考えられたのです。そこで海馬の最大線量を10Gy以下に抑制した臨床試験が米国で行われ、認知障害の発生する頻度が30%から7%に低下したと報告され大きな注目を浴びました*。海馬回避全脳照射は現在のstate of the art(最新の方法)です。
海馬トレースにおけるMRIの役割
海馬の形や大きさには個人差があります。放射線治療医は画像融合の技術等を使ってMRI画像を正確に読取って輪郭を抽出し放射線治療計画を立案します。幹細胞ゾーンは海馬本体だけでなく側脳室の壁にもあります。抽出は時間と技術の必要な作業です。私たちは長年の画像診断のキャリアがありますがそれでも正確な抽出は手間のかかる作業です。
トモセラピーの卓越性
図3Aは我々の施設のトモセラピーで計画した海馬回避全脳照射の線量分布図です。海馬以外の脳と脳脊髄液腔が均一に照射され、海馬への照射は回避されています。別の放射線治療/計画システムではどうでしょうか。図4AはElekta Infinity linear accelerator IMRTの方法で計画された海馬回避全脳照射の線量分布図で論文に載ったものです。35Gy以上照射される部分(オレンジ>35Gy、赤>37.5Gy)がまだらに存在します。
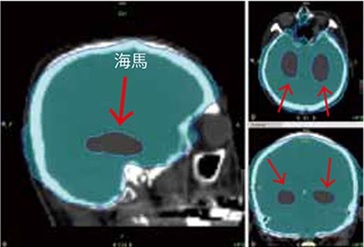
図3A トモセラピーで計画した海馬回避全脳照射の線量分布図
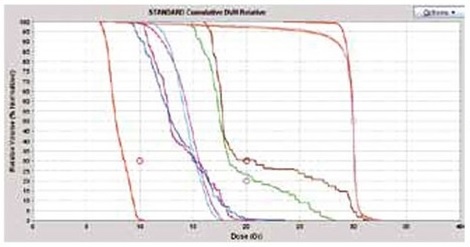
図3B トモセラピーで計画した海馬回避全脳照射の線量体積ヒストグラム
一番左の赤が海馬、10Gy未満という指示を忠実に実現できています。このほかトモセラピーでは眼球、蝸牛、視神経などへの線量を制限できています。また次に示す他施設のIMRTのように35Gy以上の照射を受ける部分はありません。
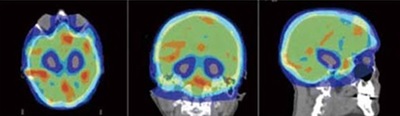
図4A Elekta Infinity linear acceleratorでIMRTの計画をした場合の線量分布図。
この論文*の主旨は、海馬回避の治療が可能、という事ですが、ところどころ赤いホットスポットができてしまっています。赤いホットスポットは必要のない障害を脳に及ぼす事になります。同じIMRTが可能な機械といっても機械によって様々のようです。
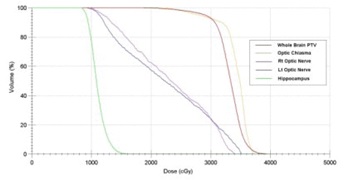 図4B Elekta Infinity linear acceleratorでIMRTの計画をした場合の線量体積ヒストグラム海馬の線量の70%は10Gy以上です。脳と脳脊髄波腔には35Gy以上照射される部分があります。
*Nevelsky A. et.al, J Appl Clin Med Phys. 2013 May 6; 14(3): 4205.
図4B Elekta Infinity linear acceleratorでIMRTの計画をした場合の線量体積ヒストグラム海馬の線量の70%は10Gy以上です。脳と脳脊髄波腔には35Gy以上照射される部分があります。
*Nevelsky A. et.al, J Appl Clin Med Phys. 2013 May 6; 14(3): 4205.
略歴「脳転移への放射線治療の選択」
いま、目の前にある治療の選択肢は、理想的な治療なのでしょうか?
あるいは現実的な選択肢の中で、本人にとってベストなのでしょうか?
このシリーズでは脳転移への放射線治療の選択をガイドします。
これまでの放射線治療は腫瘍細胞にダメージを与える事を優先してきました。そのための正常組織の犠牲もやむを得ないとして受け入れられてきました。本来、脳への照射の理想は、脳機能を守り、腫瘍を制御することでなければならない筈です。
脳への照射方法の話
この章は、脳転移への放射線治療を、選択していただけるようにお話します。第一部は、脳転移の予防のための放射線治療を、第二部は脳転位がすでにある脳転移巣の治療をお話しします。
第Ⅰ部.予防のための照射。
予防的照射
当初からあきらかな病巣がなかった領域に対して放射線治療を行うことを予防的照射と呼びます。なお、一度病巣があって何かの治療後に今は肉眼的に見えなくなった部分への照射は、予防とは呼ばずに、後治療としての照射、"アジュバント"照射と呼んで区別しています。手術で、病巣を除去した後への術後照射もアジュバント照射の一つです。予防的照射は普通は全脳に行います。
1.予防的全脳照射
脳はまだ画像的にも病巣がないが、転移が発生してくる確率が高い場合があります。それらには、限局期小細胞肺癌で肺病変が完全に制御された(完全寛解)獲得後や、急性白血病の完全寛解後などがあります。これらでは疫学的なエビデンスも十分揃い、標準治療に採用されています。
種まき元になる原発病巣が完全寛解の状態で、それでも統計的に30%以上の確率で脳転移が発生すると予測される時、その脳転移の発生頻度を予防照射で10%以下に低下させられるデータが十分あるので、標準治療になったのです。
Q and A
Q:種まき元になる原発巣が残っている場合には有益ではないのですか?
A:原発巣が生き残っている場合には照射した後の脳に腫瘍細胞が漂着するかもしれないので予防的全脳照射のよい適応とは言い難いのです。原発巣が形として残っていても腫瘍マーカーや画像診断で腫瘍細胞がほぼ死滅したと判断される場合には、CR、準CRの状態であると判断して、予防的全脳照射の適応とします。
Q:種まき元になる原発巣が残っている場合には有益ではないのですか?
A:原発巣が生き残っている場合には照射した後の脳に腫瘍細胞が漂着するかもしれないので予防的全脳照射のよい適応とは言い難いのです。原発巣が形として残っていても腫瘍マーカーや画像診断で腫瘍細胞がほぼ死滅したと判断される場合には、CR、準CRの状態であると判断して、予防的全脳照射の適応とします。
予防的全脳照射の一回線量と照射回数
総線量では、2Gyx15回=30Gyや3Gyx10回=30Gyがよく用いられます。脳機能障害等や脱毛の副作用があります。
脱毛は頭皮毛根への線量の多寡で決まります。
普通の予防的全脳照射で、海馬(近時記憶などの中枢)への照射を回避をしない場合は、30%の方に健忘などの脳機能障害が発生すると報告されています。小児の場合には就学・学習能力への影響が深刻な問題として議論されています。

図1A 予防的全脳照射法
脳の中は寄せ木細工のように色々な部分に分解できます。
海馬はタツノオトシゴのような形をしています。海馬という呼び名はタツノオトシゴを"海のお化け馬"(ÌΠΠÓΚαμΠΟς , ÏΠΠΟς = 馬 + ΚáμΠΟς = 海の怪物)というギリシア語に由来します(鼻が馬面です)。
海馬は歯状回とアンモン角からなり、大脳辺縁系に属します。辺縁系の一部とはいうものの中核的な働きをしています。新しい情報の抽出、協調、固定は海馬で行われ、新しい記憶として形成されます。海馬と大脳皮質の役割を喩えると、海馬は仕分け・関連・意義付け、そして大脳皮質が倉庫です。
海馬がうまく機能しなくなると、学習障害、近時記憶障害(昔のことは"倉庫"にあるので思い出せる)、方向や位置認識能力障害をきたします。認知症の方が場所がわからなくなるのは、この障害です。
これらの脳機能障害を起こす要因は、放射線や薬剤だけでなく、もっと一般的に、ストレス、鬱病、アルツハイマー病などたくさんあります。MRI等で、障害を起こした海馬が小さく萎縮している様子が観察されることがあります。細胞が減ってしまうと小さくなってしまうのですね。

図2 MRI画像。海馬。
http://en.wikipedia.org/wiki/File:MRI_Location_Hippocampus_up..png
Q and A
Q:予防的全脳照射を薦めないような場合がありますか?
A:あります。抗がん剤治療によって、ひどく認知能力の低下や意欲低下を来した場合です。全脳照射がその回復を妨げたりさらに悪化させたりする可能性があるからです。
Q:予防的全脳照射を薦めないような場合がありますか?
A:あります。抗がん剤治療によって、ひどく認知能力の低下や意欲低下を来した場合です。全脳照射がその回復を妨げたりさらに悪化させたりする可能性があるからです。

図1B トモセラピーでの全脳照射
脳転移は均等に分布するわけではありません。実は海馬に転移する確率は低いのです。従って海馬を外せるなら外して予防照射してはどうか、と考えられたのです。そこで海馬の最大線量を10Gy以下に抑制した臨床試験が米国で行われ、認知障害の発生する頻度が30%から7%に低下したと報告され大きな注目を浴びました*。海馬回避全脳照射は現在のstate of the art(最新の方法)です。
*RTOG米国の放射線腫瘍学グループRTOGと地域臨床腫瘍学グループCCOPの臨床試験結果、2013年9月米国放射線腫瘍学会総会
http://www.rtog.org/News/tabid/72/articleType/ArticleView/articleId/73/Avoidance-of-the-Hippocampus-Is-Shown-to-Preserve-Memory.aspx
http://www.rtog.org/News/tabid/72/articleType/ArticleView/articleId/73/Avoidance-of-the-Hippocampus-Is-Shown-to-Preserve-Memory.aspx
海馬トレースにおけるMRIの役割
海馬の形や大きさには個人差があります。放射線治療医は画像融合の技術等を使ってMRI画像を正確に読取って輪郭を抽出し放射線治療計画を立案します。幹細胞ゾーンは海馬本体だけでなく側脳室の壁にもあります。抽出は時間と技術の必要な作業です。私たちは長年の画像診断のキャリアがありますがそれでも正確な抽出は手間のかかる作業です。
トモセラピーの卓越性
図3Aは我々の施設のトモセラピーで計画した海馬回避全脳照射の線量分布図です。海馬以外の脳と脳脊髄液腔が均一に照射され、海馬への照射は回避されています。別の放射線治療/計画システムではどうでしょうか。図4AはElekta Infinity linear accelerator IMRTの方法で計画された海馬回避全脳照射の線量分布図で論文に載ったものです。35Gy以上照射される部分(オレンジ>35Gy、赤>37.5Gy)がまだらに存在します。

図3A トモセラピーで計画した海馬回避全脳照射の線量分布図

図3B トモセラピーで計画した海馬回避全脳照射の線量体積ヒストグラム

図4A Elekta Infinity linear acceleratorでIMRTの計画をした場合の線量分布図。

Q and A
Q:脳転移以外でも海馬回避は有用でしょうか。
A:有用です。原発性脳腫瘍のひとつである悪性膠芽腫でも有用という報告が2014年に発表されています*。 *Ali AN, et.al. Radiat Oncol. 2014 Jan 10;9:20.
Q:脳転移以外でも海馬回避は有用でしょうか。
A:有用です。原発性脳腫瘍のひとつである悪性膠芽腫でも有用という報告が2014年に発表されています*。 *Ali AN, et.al. Radiat Oncol. 2014 Jan 10;9:20.
岸 和史(きし かずし)
1983年和歌山県立医科大学医学部医学科卒業後、同大学助手(放射線医学講座)、講師、助教授、准教授を経て2013年医療法人北斗 北斗病院放射線治療科部長、2014年より副院長、現職。
この間1997年米国テキサス州立大学MDアンダーソン癌センター実験放射線腫瘍学教室にPostdoctoral Fellowとして留学
日本放射線腫瘍学会認定医、放射線治療専門医、医学博士
1983年和歌山県立医科大学医学部医学科卒業後、同大学助手(放射線医学講座)、講師、助教授、准教授を経て2013年医療法人北斗 北斗病院放射線治療科部長、2014年より副院長、現職。
この間1997年米国テキサス州立大学MDアンダーソン癌センター実験放射線腫瘍学教室にPostdoctoral Fellowとして留学
日本放射線腫瘍学会認定医、放射線治療専門医、医学博士

