『核医学診療推進国民会議を設立した理由』
金沢大学医薬保健研究域医学系核医学教授
絹谷 清剛
内用療法は日本では本文中にあるように現在6種のがんに対する診療(治験などを含む)が行われているそうだが、 現在開発中のものは希少がんに対するもので、多数のがん患者にとっては遠い存在で関心も薄い。
だが、世界ではあらゆる臓器原発のがん腫に対する治療が、様々なレベルで臨床検討されているそうで、 ご寄稿いただいた絹谷先生によれば「日本の核医学は世界のレベルから1周後れどころか欧米はもちろんアジア・アフリカ諸国にも後れをとり、2周後れになっている」そうで、 治療を受けたい日本人がヨーロッパや東南アジアなどに行って治療を受けているそうである。
16年ほど前に当会が発足当時初めて患者会が共同して患者の声を厚労省などにアピールしたとき、 地方では受けられない治療を受けるためにわざわざ飛行機で地方から東京に通って来ていた患者会のリーダの一人が日本中どこでも受けたいがん治療が受けられるようにと強く訴え、 「がん治療の均てん化」が実現したが、この時は抗がん剤の早期承認と早期保険収載が目標だった。
核医学も同様ではないか、もっとその治療についての情報を広く発信し、多くの市民の皆様と共に核医学によるがん治療の早期承認を実現しようではありませんか。
今回はこの問題について核医学診療推進国民会議会長で金沢大学医薬保健研究域医学系核医学教授の絹谷清剛先生にご寄稿いただきました。
核医学診断・治療とは
核医学とは、放射線を出す医薬品(放射性医薬品)を患者さんの体内に投与させていただいて、診断・治療を行う医療です。 核医学という言葉は初めて耳にされた方でも、PET(ポジトロン放射断層撮影)によるがんの検査を受けた方が多くおられると思いますが、PETは核医学診療のひとつです。
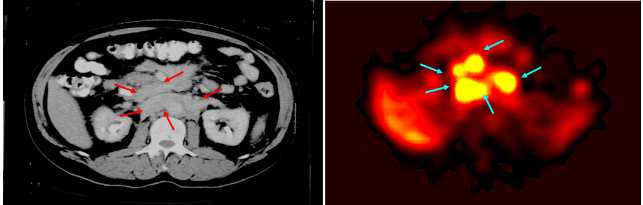
図1 左図はX線CT、右はある放射性医薬品を用いたシンチグラム断層像。矢印ががん病巣。X線CTで腫瘍の見られる部位に、放射性医薬品が集積しています。
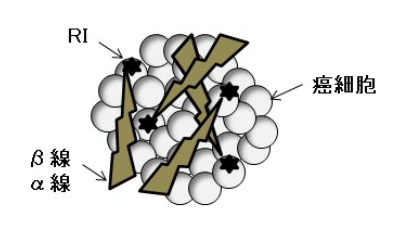
図2 核医学治療のイメージ
ガンマ線あるいはポジトロンを放出する放射能(一般にアイソトープRIと呼ばれます)をつけた放射性医薬品を作ってがん組織に集まるように設計すれば画像(シンチグラム、PET)をとってがん診断ができます(図1)。 一方、ベータ線やアルファ線を放出するものをつければ、がん組織にこの薬剤が集まり、がん細胞を放射線で叩く放射線治療ができます(図2)。 この治療を核医学治療(内照射療法、内用療法、アイソトープ治療とも呼ばれます)と呼びます。 昨今、がん細胞が細胞の表面に出している物質などを標的に用いてがん細胞を叩く分子標的薬と呼ばれる治療薬が多く使われますが、 核医学治療はその手法を応用して放射線でがん細胞を叩くというイメージで考えて下さい。 放射能を体に投与すると聞くと、なにやら恐ろしい感じをもたれるかもしれませんが、がん組織に集積しない部分は主に尿路系から尿中に速やかに排泄されますので、安全な治療と言えます。 通常の抗がん剤の治療では、治療中に吐き気・おう吐などのつらい時間がありますが、核医学治療ではこのようなことは多くの場合ほとんど生じません。 したがって、通常の治療よりも体にやさしいと言ってもよいかと思います。
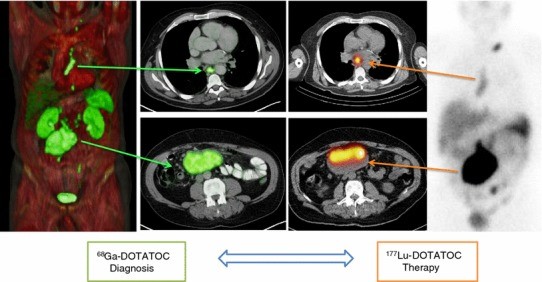
図3 悪性神経内分泌腫瘍治療における核医学theranostics。 左図は診断用放射性PET薬剤68Ga-DOTATOCであらかじめ病巣への集積を確認したもの。 右図は治療用放射性薬剤177Lu-DOTATOCで治療中に177Luからでるγ線で撮像したもの。 診断時の画像と治療時の画像の同一性に注目してください。参考文献1から転載許可。
核医学の治療は、甲状腺機能亢進症(バセドウ病・グレブス病)の治療から始まり、すでに80年近い歴史を有します。 その後、甲状腺癌等々の種々の種類のがんの治療に広がりをみせてきました。 さて、前段で、診断と治療の話が出てきました。 この二つを、同じ物質で行ったとしたらどうでしょうか。 つまり、ガンマ線・ポジトロンを出すアイソトープで診断をして、その後にベータ線・アルファ線を出すアイソトープで置き換えてやれば治療ができますね。 このように治療計画を立てれば、この薬ががん組織に集まることを事前に確認することができ(有効性の面での患者選択)、 どれだけがん組織に集まったか測定(線量計画)でき、どのような治療効果が期待できるか予測(効果予測)できることになります。 投与した患者さん体の中の薬剤の広がりが通常とは異なると副作用がでる恐れがありますが、核医学治療ではあらかじめ画像化することによりそのような危険性を回避することも可能です(安全性の面での患者選択)。 治療後には、同じもので診断を行えば、効果判定や経過観察が可能です。 昨今このような一連の流れ・概念を、theranosticsという造語で表現します。 この言葉は、治療を意味するtherapeuticsと、診断を意味するdiagnosticsを掛け合わせたものです(図3)1)。
プレシジョン医療
さて皆さんは、個別化医療、テーラーメード医療という言葉を聞いたことはありませんか。 最近では、アメリカの前大統領オバマ氏が使ったプレシジョン医療という言葉の方がなじみ深いかもしれません。 一般には、がん医療におけるプレシジョン医療(precision medicine)とは、個々のがん患者さんの体内にあるがん組織に特異的な遺伝子情報を解析することにより、 個々の患者さんである治療が有効であることを検索した上で治療を行うことを意味しています。 非常に合理的な考えで、これでがん診療がバラ色になるように思えます。 しかし、現在使用されているがん診療における分子標的薬を眺めると、奏功率は数十%にすぎず、どれだけの医療資源が無駄に費やされているのか想像も困難です。 さらに、有効性の面における患者選択に主に目が向かっている現状の視点は、それはそれで大きな意義があることに間違いはありませんが、 副作用回避の視点にも重きを置かない限り、お題目倒れであると思います。 これらを背景に考えると、プレシジョン医療を成功させるためには、がん病巣への標的薬の集まりを確認するとともに、不適切な体内分布になっていないかを確認することが求められると思います。 つまりは、標的薬そのものの画像化が必要であり、このような目的に核医学画像がコンパニオン診断として使用することが考えられています。 この段で議論した治療薬は放射性医薬品ではありませんが、これを放射性医薬品で行ったとするならば、遺伝子情報でまず患者選択し、画像を撮って病巣にしっかり集積することを確認すると同時に、 性状臓器に望ましくない分布になっていないことを確認した上で治療実施が可能です。 前段で説明したtheranosticsとprecision medicineを融合すると、個別化医療を一段高みに揚げることができると思います。 最近私はこのような概念を、precision nuclear medicine、precision nuclear theranosticsなどと表現しています。
核医学治療の世界的現状と日本の立ち位置
- 甲状腺分化癌 (131I)
- B細胞性悪性リンパ腫 (Zevalin®, 90Y-anti-CD20)
- 去勢抵抗性前立腺癌骨転移 (Xofigo®, 223Ra)
- 褐色細胞腫・傍神経節種 (131I-MIBG 企業治験I/II相、金沢大学)
- 化学療法不応性神経芽腫 (131I-MIBG 先進医療、金沢大学)
- 神経内分泌腫瘍 (117Lu-PRRT 企業治験I/II相)
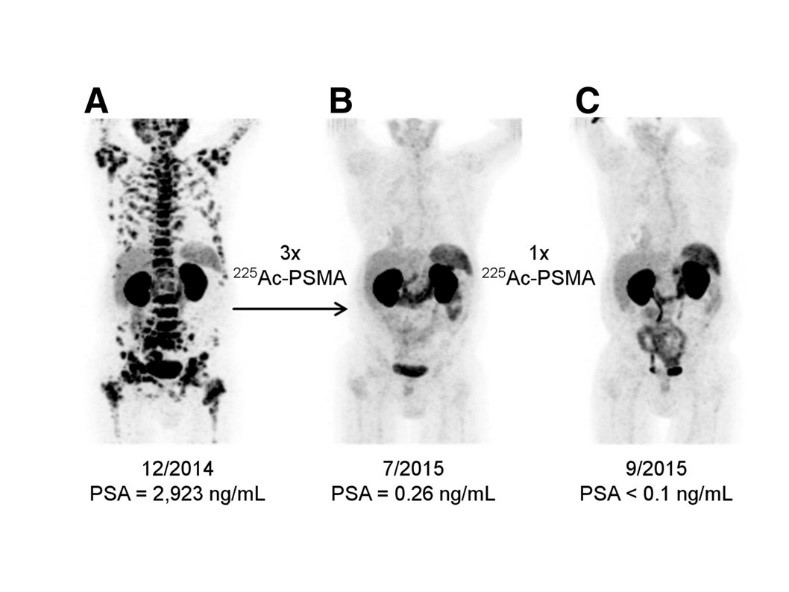
図4 前立腺癌全身多発転移患者における核医学治療例。 治療前に全身多発転移があり抗がん剤などが無効であった患者が(A、治療前)、 α線核種225Ac-PSMAによる計4回の治療でほぼ寛解となっています(C、4回の治療後)。 参考文献2から、転載許可。
現在我が国で実施可能な癌に対する核医学治療を表1にまとめました。 表には現在治験や先進医療で実施されているものも記載しましたが、両手にも満たない数にすぎません。 一方、世界に目を転じると、あらゆる臓器原発のがん腫に対する治療が、様々なレベルで臨床検討されています。 欧米ではすでに診療ガイドラインに組み込まれ、アジア・アフリカ・南米の諸国でもすでに広く実施されている有効性の高い核医学治療(図4)2)が、 我が国においてはようやく開発段階(治験)にある状態か、一切開発が進んでいない状態にあります。 その結果、当該疾患の多くの患者さんが、海外に治療を求めて渡航しておられます。 スイス、ドイツ、オーストラリアに加え、昨今マレーシアへも患者が訪れているのが現状です。 どうしてこのような状況に陥ってしまったのでしょうか。
核医学治療の国内開発を妨げるバリア


図5 金沢大学附属病院の放射線治療病室。上図は病棟入り口。下図は病室内。一般の病室と変わりありません。
医療は、単純化して言うと、法的には医療法の中で行われるものです。 また一般薬の開発には薬機法という法律が関与し、薬機法で承認が得られると医療法で用いられるというステップをとります。 一方、放射性医薬品開発ではこれらの法律に加え、原子力規制庁管轄の放射線障害防止法と従事者被曝を管理する労働安全衛生法が大きく関与します。 さらには、昨今世界的に開発が進んでいるアルファ線放出アイソトープは、多くの場合原子炉等規制法という非常に厳しい法律に縛られ、我が国における開発は著しく困難な状況にあります。
また、少なからぬ種類の核医学治療では、治療時に専用の放射線治療病室(アイソトープ病棟)(図5)が必要です。 しかし、治療室は現在日本全体で約150床前後しかなく、この病床は甲状腺癌核医学治療でほぼ飽和しており、新規治療開発が簡単にできる状況にはありません。 核医学治療開発の最先端国のひとつであるドイツでは、人口約8000万人に約2000床(20年前のデータ)存在しています3)。 日本の病床が少ないのは、治療実施に対する診療報酬が十分でないことが主因です。 治療施設の維持に関わる経費(ランニングコスト)もまかないきれない非採算部門であるため、治療病室を閉鎖する病院もあるくらいです。
対策・皆さんにお願いしたいこと
日本核医学会の長年にわたる行政への働きかけにより、この悪環境は緩やかにではあるものの改善の兆しを見せ始めています。 従来は、未承認放射性医薬品は、障害防止法の規制のためほぼ臨床の場で使用することができませんでしたが、 現在、診療に用いるものは未承認薬であっても、ある手順を踏めば医療法だけで取り扱うことができるような方向に規制の一部緩和が行われました。 しかしまだまだ多くの障害が残存しています。
核医学治療で世界をリードしているのは欧州、オーストラリア、米国です。 これらの国はどのように開発を進めているのでしょうか。 前述の規制の問題が我が国のように存在しないのかもしれませんが、それ以上に重要な要素であると考えられることは、国が医療施策の中で核医学診療をしっかりとサポートしていることです。 ヨーロッパではEuropean Commission4)、米国ではDepartment of Energy5)、 オーストラリアではAustralia's Nuclear Science and Technology Organisation6)が長年にわたって医療用アイソトープ生成の要望を医師・研究者と議論しながら、核医学治療開発を進めています。 カナダも昨年、首相が医療用アイソトープ生成センターを国が施策としてサポートする旨を公表しました7)。 核医学治療の開発・推進のためには、原子炉・加速器などの大型装置が必須で、アカデミアや企業のみの自助努力で運営することはほぼ不可能です。 したがって、このような国の関与が必要なのです。
我が国では、平成27年の衆議院国会に提出された核医学治療に関わる主意書に対して、安倍首相が “放射性同位元素による内用療法を含む放射線療法の更なる充実については、 「がん対策推進基本計画」においても重点的に取り組むべき課題としており、政府としては、引き続き研究開発の推進等の取組を進めてまいりたい” と答弁されました。 また、厚生労働省が発出した第3期がん対策推進基本計画(平成29年10月)やがん診療連携拠点病院等の整備に関する指針(平成30年7月)の中に、 初めて“核医学治療”の文言が記載され、国がその重要性を認識し始めています。 現在、医療法核種はほぼ輸入に頼っており、過去に生じた世界的供給トラブルの結果、診療に支障を来したことを幾度も経験してきました。 これまでも、国内合成を繰り返し議論してきたものの進捗は見られませんでしたが、これを進めるためのプラットフォームとして、一般社団法人日本医用アイソトープ開発準備機構(JAFMID)が設立されました8)。 厚生労働省、通商産業省、文部科学省、原子力規制庁等の関連行政を一緒になった議論が期待されているところです。
2年前に、患者・医師・研究者・関連企業が一つになって、世界で行われている核医学治療の国内導入を推進するため本会核医学診療推進国民会議9)を設置し、 行政に対するアドボカシー活動を開始したのは、前述のような日本のがん患者さんがうけている不利益を改善し、新たな治療選択肢を適切なタイミングで提供することができる環境を整えるためです。 座視すれば、我が国のがん患者に世界標準治療を提供できないことになりかねません。皆さんと一緒に活動できることを祈念しています。
参考文献
- Werner RA, et al. 68Gallium- and 90Yttrium-/ 177Lutetium: "theranostic twins" for diagnosis and treatment of NETs. Ann Nucl Med. 2015 Jan;29(1):1-7.
- Kratochwil C, et al. 225Ac-PSMA-617 for PSMA-Targeted α-Radiation Therapy of Metastatic Castration-Resistant Prostate. J Nucl Med. 2016 Dec;57(12):1941-1944.
- Hoefnagel CA, et al. Radionuclide therapy practice and facilities in Europe. EANM Radionuclide Therapy Committee. Eur J Nucl Med. 1999 Mar;26(3):277-82. Cancer
- http://ec.europa.eu/euratom/observatory_radioisotopes.html
- https://science.energy.gov/np/research/idpra/
- https://www.ansto.gov.au/
- https://www.triumf.ca/headlines/prime-minister-canada-announces-establishment-premier-centre-for-advanced-medical-isotope
- https://www.jafmid.or.jp/
- https://www.ncnmt.jp/
1986年金沢大学医学部卒業後北陸中央病院内科、金沢大学医学部核医学診療科などを経て2006年金沢大学医学部附属病院核医学診療科講師、 金沢大学医薬保健研究域医学系 核医学 教授 2012年より金沢大学附属病院副院長、2013年より福島県立医科大学特任教授
2014年より放射線医学総合研究所放射性同位元素内用療法に関する検討委員会委員
この間1990年より米国国立衛生研究所クリニカルセンター核医学科フェロー
学会:日本核医学会(理事)日本医学放射線学会(代議員)日本内分泌外科学会(理事)日本甲状腺学会(理事)など
賞罰:2002年Springer Prize 2002 (Best Science Paper, European Journal of Nuclear Medicine)ほか多数

